¡Nunca faltan los dramáticos en el laboratorio!



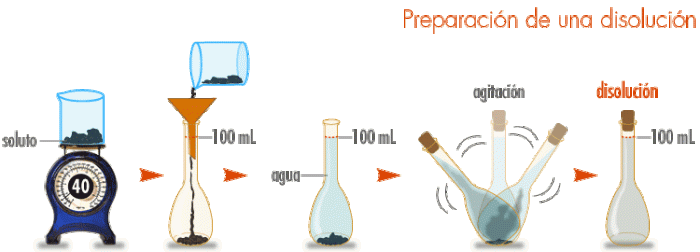
Cuando nos sirven un vaso de jugo de naranja y este está muy concentrado, por lo general si no nos gusta así, lo que hacemos de forma automática es añadir más agua, de manera tal que el sabor del jugo sea de nuestro agrado, es decir, le bajamos la concentración a la bebida. Esta técnica que ejecutamos de manera instintiva, se le llama dilución.
La dilución es el proceso de preparación de una solución de menor concentración a partir de otra de mayor concentración, agregando solvente. En las disoluciones, la cantidad de soluto no varia, lo que cambia es el volumen de solvente, ya que a medida que se añade más solvente, la cantidad de soluto disminuye, debido a que el volumen y masa de la solución aumenta. Leer más…«Dilución. Ejercicios Resueltos»

Esta propiedad se encuentra relacionada con el fenómeno de la ósmosis. La ósmosis es un proceso natural muy frecuente en la naturalea, relacionado con los procesos de nutrición de los seres vivos. Este consiste en el paso de solvente de una solución que contiene poca cantidad de soluto hacia otra con mayor cantidad de soluto, en búsqueda de un equilibrio, es decir, igualar las concentraciones a través de una membrana semipermeable.Leer más…«Propiedades Coligativas: Presión Osmótica»
La fracción molar relaciona el número de mol de soluto con el número de mol total presente en solución. Se designa con la letra X y no presenta unidades.
X = X soluto + X solvente = 1
X = Fracción molar
X soluto (Xsto) = Fracción molar del soluto
X solvente (Xste) = Fracción molar del solvente
La suma de las fracciones molares del soluto y solvente es igual a 1
La molalidad se refiere al número de mol de soluto que se encuentra disuelto en un kilogramo de solvente. Por lo tanto, su unidad es mol/kg y se designa con la letra “m” minúscula. Por ejemplo: Si una solución presenta una concentración 5 molal, significa que contiene 5 mol de soluto en cada kilogramo de solvente. La expresión matemática empleada para calcular la molalidad es:

Las unidades químicas a diferencia de las unidades físicas de concentración, relacionan el mol de soluto que presenta las soluciones, en este caso, que estudiaremos la molaridad (mol/L), el mol se relaciona con el volumen de la solución en litros.
Se define como la cantidad de mol de soluto entre el volumen de la solución en litros. Se designa con la letra M mayúscula, aunque en la actualidad se le conoce como simplemente concentración mol/L.
La fórmula que se utiliza para calcular la concentración molar es la siguiente:

O en la fórmula desarrollada: M = gramos de soluto
Masa molar x V (L)
M = ?
g soluto = 25g
g solvente = 350g
ρ = 1100 kg/m³
Masa molar del NaOH = 40 g/mol
M = gramos de soluto
Masa molar x V (L)
Si observamos la fórmula anterior, sólo disponemos de los gramos de soluto y la masa molar para calcular la molaridad y es necesario buscar el volumen de solución; para ello lo relacionamos con la densidad. Entonces partimos de la fórmula de densidad, la cual no es más que la relación entre la masa y el volumen de la solución. Así que primero que nada buscaremos calcular la masa de dicha solución sumando la masa del soluto con la masa del solvente, quedando así:
m solución = m soluto + m solvente
m solución = 25 g + 350 g
m solución = 375 g
Ahora bien, como tenemos la densidad y la masa de la solución, se puede despejar de la fórmula el volumen:
ρ = m/ v
V = m/ ρ
Como la densidad está en Kg, transformamos la masa de la solución de gramos a kilogramos y nos queda igual a 0,375 Kg. Sustituimos en la fórmula:
v = 0,375 kg / 1100 kg/m³
V = 0,000341 m³
1 m³ equivale 1000 litros, entonces queda igual a 0,341 litros.
M = 25 g
40g /mol x 0,341 L
M = 1,83 mol/L
2. Calcular los gramos de HCl que se requieren para preparar 500 ml de solución al 0,5 M.
g soluto = ?
V solución = 500 ml = 0,5 L
M = 0,5 mol/L
MM HCl = 36,46 g/mol
gramos de soluto = M x Masa molecular x V (L)
gramos de soluto = 0,5 mol/L x 36,46 g/mol x 0,5 L
gramos de soluto = 9,12 g de HCl