Cuando hablamos de enlace lo asociamos rápidamente con la unión, combinación, acoplamiento en este caso de átomos para formar moléculas y macromoléculas. Pero, ¿por qué se enlazan los átomos?
Lo que sucede es que cuando un átomo se halla solo, cada electrón que lo conforma, experimenta la influencia de su núcleo y de los restantes electrones, sin embargo cuando dos átomos se aproximan y se enlazan, los electrones correspondientes a cada átomo (no cualquier electrón, puede formar un enlace, sino solamente los electrones del último nivel energético, es decir, el más externo) están sometidos a la influencia del núcleo y de los electrones del otro átomo. Por lo tanto la fuerza de atracción que existe entre esos átomos se denomina enlace químico.
Existen diferentes tipos de enlaces químicos que se dan dependiendo del tipo de compuestos. Estos enlaces pueden ser: iónicos, covalente, dativo y metálico.
Enlace Iónico
Es la fuerza que permite la unión de dos átomos a través de una transferencia electrónica. Dicha transferencia se lleva a cabo cuando un elemento electropositivo se une con un elemento electronegativo. El enlace iónico será más fuerte a medida de que la diferencia de electronegatividad entre los elementos sea mayor. Se considera que es un enlace iónico, cuando la diferencia de electronegatividad entre los elementos involucrados es mayor a 1.7.
Ejemplo:
NaCl Cloruro de sodio
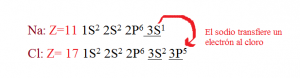

Enlace Covalente
Es la fuerza que permite la unión entre dos átomos mediante la compartición de un electrón por átomo. A su vez los enlaces covalentes se dividen en enlace covalente polar y apolar.
Los enlaces covalentes polares son aquellos en donde la diferencia de electronegatividad de los átomos que lo forman va desde 0 hasta 1.7 (sin considerar el 0). Presentan un momento dipolar distinto a cero, además de ser solubles en agua y otros solventes polares.
Por su parte, los compuestos que se originan por medio de enlaces covalentes apolares, no exhiben momento dipolar y la diferencia de electronegatividad es igual a cero. Este tipo de compuesto presenta simetría y son solubles en solventes apolares, como por ejemplo el hexano.
Ejemplo:
Metano
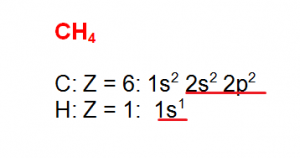
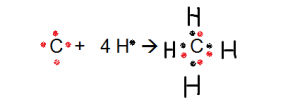
Enlace Dativo
Este enlace se caracteriza por presentar un par electrónico que es cedido por un sólo átomo, el cual debe tener al menos un par de electrones libres sin enlazar. Por ejemplo como el nitrógeno, oxígeno y cloro.
Igualmente, el átomo que acepta el par electrónico debe estar carente de electrones, como el ión hidrógeno y el aluminio, por ejemplo.
Ejemplo:
NH4+ Ion amonio
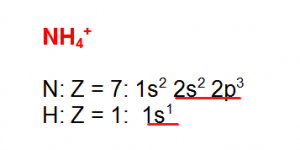
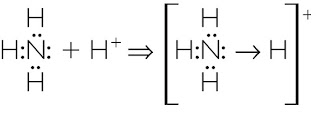
Enlace Metálico

Este tipo de enlace se caracteriza por la unión de metales, mediante la pérdida de electrones de sus capas más externas, que se reubican más o menos libremente entre ellos, creando una nube electrónica.
Estos átomos se concentran de manera muy cercana unos a otros, lo que ocasiona estructuras muy compactas. Un ejemplo, son los característicos empaquetamiento compacto de esferas (hexagonal compacta), cúbica centrada en las caras o la cúbica centrada en el cuerpo.
Ejemplo:
Los enlaces metálicos son sumamente frecuentes en el mundo atómico de los metales, por lo que cualquier elemento metálico puro es un ejemplo posible de los mismos, a saber:
- Enlaces entre los átomos de Plata (Ag).
- Enlaces entre los átomos de Oro (Au).
- Enlaces entre los átomos de Cadmio (Cd).
- Entre otros.


Excelente
Pingback: Polaridad en el enlace químico. Ejercicios Resueltos - Química en casa.com
Looking for something exciting? This website has it all: www [dot] porncastelo [dot] com
Fantastic goods from you, man. I have understand your stuff prior to and you’re simply too fantastic. I actually like what you have bought right here, certainly like what you are stating and the way in which by which you are saying it. You are making it entertaining and you still take care of to stay it sensible. I can’t wait to read far more from you. This is actually a terrific website.
I loved up to you’ll obtain performed right here. The comic strip is attractive, your authored material stylish. nevertheless, you command get got an edginess over that you wish be handing over the following. unwell for sure come further formerly once more since precisely the similar nearly very frequently within case you defend this hike.
What¦s Happening i’m new to this, I stumbled upon this I’ve found It positively useful and it has aided me out loads. I hope to contribute & assist other customers like its helped me. Good job.
Excellent post. I used to be checking constantly this weblog and I’m impressed! Very helpful info specially the last part 🙂 I take care of such information much. I was seeking this particular info for a long time. Thank you and good luck.