Probablemente hayas escuchado la palabra luminol en algún programa de televisión policíaco como por ejemplo CSI, donde observamos a los forenses revelar rastros de sangre para tratar de resolver casos de homicidios.

El 5-amino-2,3-dihidroftalazina-1,4-diona es el nombre dado por la IUPAC para el luminol, el cual es un compuesto químico que produce quimioluminiscencia, es decir, emite una luz azul al ser combinado con un agente oxidante apropiado, usualmente con peróxidos ya que presentan enlaces oxígeno-oxígeno y ostentan una valencia de -1 en dicho elemento.
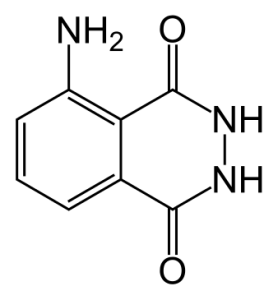
Este compuesto químico es utilizado ampliamente por los científicos forenses para tratar de resolver crímenes de naturaleza violenta. Pero, ¿cómo actúa el luminol en presencia de la sangre?
Los químicos forenses preparan una disolución de peróxido de hidrógeno y de luminol, luego se oscurece la habitación y se aplica en la zona donde se tiene la sospecha de que hay rastros de sangre. Si en dicha zona hay sangre, la disolución preparada reaccionará con el hierro en forma de catión que se halla en el grupo hemo de la hemoglobina y actuará como catalizador a la reacción, lo cual permitirá que el lugar se ilumine de un color azul durante unos 30 segundos. La luminiscencia se puede observar perfectamente en lugares oscuros.

Hablando en términos químicos, lo que ocurre es lo siguiente: el luminol es oxidado para formar un dianión, el cual tiene enlaces de amida que originan el anión de ácido 3-aminoftálico en su triple estado excitado. Los electrones excitados pasan del estado singular al estado basal. En esta etapa se produce una luz azul a una longitud de onda de 485nm en un medio aprótico y a 425nm en un medio prótico. Cuando se absorbe luz ultravioleta o visible, se origina un electrón que pasa de estado basal a un estado excitado singular, es decir, un estado en donde los electrones están apareados. Luego en un lapso de tiempo de 10 a 11 segundos, el electrón desciende a un estado excitado singular de menor energía.
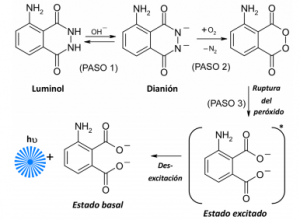
Ahora bien ¿Es eficaz utilizar el luminol para solventar crímenes?
La actividad peroxidasa al utilizar luminol, origina una serie de inconvenientes que pueden limitar su aplicabilidad en una investigación, ya que puede originar falsos positivos. La reacción de luminiscencia puede ocurrir en presencia de algunas sustancias como: metales (cobre), jugos de fruta, detergentes, blanqueadores, orina, materia fecal, entre otros.
Pero si es utilizado de manera adecuada y por un científico forense experimentado se podrá sacar provecho de este maravilloso compuesto químico. De hecho un investigador veterano, con tan solo observar la velocidad de la reacción química puede juzgar si la sustancia es sangre o no.



Has dado en el sitio con este post , realmente creo que este blog tiene mucho que decir en estos temas . Volveré pronto a vuestro blog para leer mucho más , gracias por esta información .
Muchas gracias a ti Carmen por tu apoyo, saludos 🙂
Pingback: ¡Una reacción muy brillante! - Química en casa.com
News from the staff of the LA Reporter, including crime and investigative coverage of the South Bay and Harbor Area in Los Angeles County. https://lareporter.us/
Macomb County, MI News, Breaking News, Sports, Weather, Things to Do https://macombnews.us